|
|
(文中数据皆为暂估数,需要依据原有数据统计并参考外部标准确定后试行)" D/ J$ A- K: O
第一章 总 则
" p2 e, Q b9 ~0 Y: r6 ? 1 y% }* Q- m O+ K2 W* Q
第一条( g) |! K0 a) z3 Q* C
3 Y! g5 ^5 D) p0 ^9 [
1:目的
l" P6 f& N5 |# |+ i - e# D/ }5 D2 v* G
1.1:为了更好的提高研发效率,让圣和的研发人员能更高效的创造出更安全有效的药物;
9 c0 H& M- P& Q$ o+ l( ^ , [ c! N1 x% T4 @' S4 N" E7 L4 }
1.2:为奋斗者合理分享其创造的价值
6 u M+ J% ?- L) j' A; j" H
2 h" `* C, x0 D' H( W6 d8 }1 y1.3:实现合理的研发成本控制,增强企业的市场竞争力,实现企业可持续发展。3 Y* Y- m: g. h
& E4 M5 f9 w* r' i$ h1.4:本着追求合作,创新,严谨,认真,勤奋的工作方式,同时为研发人员任职资格评审、职位升职、聘任等提供依据,结合研发中心实际情况,特制定本管理办法。
3 ^/ C5 `" L' C4 h$ s ! n7 Z+ A% |3 h9 P' t; H% K( ^" j" U/ C% r
2:该办法的思路和管理理念; W: e0 `5 C: W& J
/ K u- u( m5 \9 w/ j9 {+ S. J# a2.1:以项目为主线,一切围绕项目展开各项工作+ a O7 c# x: |9 z [2 L9 h& ]0 e
" T2 _, C; k/ E5 G0 I8 A$ R2.2:以项目组为中心,其他各部门围绕项目组做好各项服务工作
+ E0 Y6 Q8 [: b4 [3 K r4 `1 _6 J
! d& A: c5 M* J$ L' o! z2.3:以技术为主导,行政围绕技术给予服务、帮助和支持
" u2 }+ t V5 u( i6 S& i " H" u1 e! Q2 `6 t" o9 J
2.4:项目组经理的行政职务的职责主要是起到整合资源,统一组织项目的实施和推进的作用
3 T5 ]( [! u8 |3 a 3 T% f8 w0 l5 R4 s5 A
第二章
% o9 P& j3 c4 h p: v E- o. i n1 U; ]1 {% C
第二条:项目的研发方向:
1 N" m3 p" ]6 o4 W9 ?6 s! g
4 q/ n/ Y, G# k/ s6 a7 O. u1:已发现的疾病,但目前市场上的药物尚无法治愈的药物;
# d, Z* X% p* d q$ H
# E! i' Y3 ?9 y5 h: L' z3 w2:能对已上市的药物安全、有效性存在较大缺陷的改进的药物8 Z( z7 v* Z }) Z$ i4 u4 S
. w. C% }# r1 Q M( k& d
申请与立项2 F7 n6 P$ X! k/ ?" o" P
- P! S9 D$ F! B! M
第三条 项目的申请由研发中心高级研究员以上的研发人员按以上研发方向负责提出申请,由项目管理部负责组织评审。 @/ d9 F: \" B% U4 O3 F1 T# k
( x) @7 Z7 F3 a5 k第四条 每年高级研究员需通过立项的创新药项目不得低于0.5个,资深研究员需通过立项的创新药项目不得低于1个,各专业首席科学家通过立项的创新药项目不得低于2个,首席科学家通过的创新药项目不得低于3个,非创新药项目及微创项目2个折合一个创新药。/ C* v$ J' j3 [" _+ }) ?- ]
* a. K4 W) ~" ?: {6 o1 u第五条 项目管理部每个季度负责组织研发项目的立项的评审工作,
" F/ a1 M" G& {0 K% L; \1 o. V 4 i; |. I2 U6 ^
第六条 鼓励高级研究员以下的研发人员及其他员工提出项目立项申请。
& i9 W/ p8 x. V9 P B2 C
m; d# M. ~0 g: \) Z3 a第七条 申请立项的项目需满足:1:预测上市时具有技术先进性;2:在同一类产品中,按占该类药物的平均市场份额计算的国内市场容量存在不低于5亿。/ O) J( _" z1 B
- U2 b' N' U. p; [
第八条 非列为年度考核指标的人员提出的项目,立项申请一经公司采用,创新药给予5000到10000元的奖励。) G4 {* l2 R4 t7 a% }
+ ?; Y4 o8 F/ G2 L/ c6 ~6 j
第四条 项目立项申请人向项目管理部提出立项申请。一个月内由项目管理部组织市场部、销售部、商务部、研发中心各业务部门及外部专家进行评审。项目管理部汇总评审意见,并出具评审报告,最终报研发中心项目立项评审委员会决定是否同意立项。
, y' A3 C0 [) h. U$ u4 f6 i
. @" q) w6 Q g U7 `! O" g第五条 研发中心立项委员会由公司总经理、研发中心负责人、市场部、资深研究员以上技术人员、以及相应的外部专家组成。
" }8 J7 O" y+ W+ ]
n$ x' J9 W( ]' C& n: @& ]( W9 F第三章 项目的日常管理与职责. w# \3 O1 | I2 F( |
第六条 项目管理主要由科研项目评审委员会、研发中心负责人、项目经理、项目管理部分层、分级开展。
4 ~6 s9 f c) w# m% @4 U6 b+ |
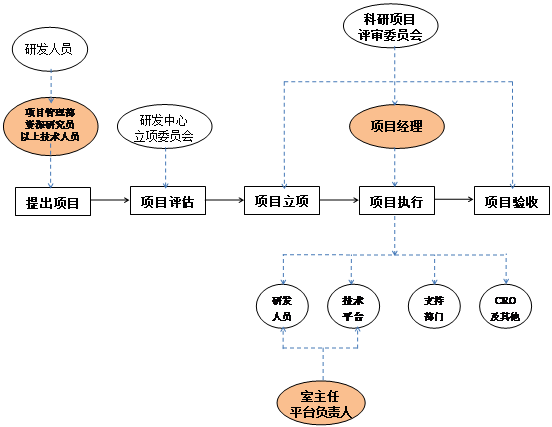
5 t; Y1 ~2 x. F8 z' x: _) p 项目立项及管理流程如下:
2 }6 F1 ^! i9 f3 A5 R. @0 w
 : ~) X0 ^3 S4 `% R, G4 Y
: ~) X0 ^3 S4 `% R, G4 Y
第七条 科研项目评审委员会由总经理、研发中心负责人、项目管理部、市场部、商务部、注册部、生物部、财务部、项目经理及下一阶段项目经理及外部专家组成,其主要职责包括:/ F' p' e! ?/ q( Q$ {* f
1)审核项目的立项书及考核项目经理;
, l8 g' o* M& H% H) j! K2)对项目的立项、推进、终止等进行决策;% w2 v3 k8 G7 m" m
3)对项目推进过程中的节点计划变更作调整给予批准;
( F/ b4 n% u7 x, m. O& x7 W2 q# Z第八条 项目管理部职责
7 t* f: `" x' a; U 6 @% ~" @# z0 H* y
项目管理部为研发中心项目管理的职能部门,负责研发项目的全过程管理。
& ?; E' x4 X* z7 |1)负责项目立项、实施、验收过程中各项活动(会议、评审、验收、论文编选等)的组织与管理;
* B/ |6 l' i) U9 y6 @7 I2)负责组织项目组经理及项目组成员选拔与变更管理;
8 F4 G5 j$ N2 U) q3)负责各项目的专利风险评估及专利战略制定;: ~* H; H6 q8 p) `" j [
4)负责各项目任务书、计划书、总结报告、各项汇报与报表的搜集与汇总,并且建档与保管;
' l4 ~9 O3 e" A! b! ^, T& s5)负责组织项目实施过程与进展的监督、检查,协调并处理项目执行过程中出现的有关问题,向研发中心负责人汇报项目月、季、年度执行情况;
: j$ f J( } @/ T5 y6)各节点完成后,按要求负责组织与整理项目验收的有关文件资料准备,向研发中心负责人汇报,并上报科研项目评审委员会进行项目验收。, n6 b( b' L0 N1 X4 \- L4 Q" d* a
第九条 市场部职责+ d8 u* R9 [" o* b* Y0 z6 |
" y: Q$ `$ k9 L* X1)对申请立项项目进行市场预期预测,给出是否立项的建议;; ]8 S* C! w" E [0 y
0 C i: Y& N+ j0 d7 u ^
2)已立项的项目及时根据当前市场动态,预测判断项目的即时市场风险,并按时间节点给出市场即时风险评估报告;/ M* z& R ~ ]1 p* [$ c# _
2 g; k' I g& C7 N# A, e* ?- z
第十条 商务部职责7 H3 a+ _ z. P& ~
5 \# q" ^, T+ }; ?4 c# E
负责预测项目上市时产品的价格,以及产品上市后,由于市场份额竞争可能带来的价格预期。
" y# R# K' _" T( i2 I
( A( X8 `5 y8 x4 l* N第十一条 注册部职责+ u2 @9 B( _9 n( m6 R
8 ^+ q4 p1 S: P2 w; F! Y, C& W2 ^, s1)主要预测项目的审批上市时间及审批数量;5 ^3 a3 t( T" B; \* ]- I
( |# g: `# a3 ]2)对申报材料审查是否符合申报要求;) g# `* S* n6 [) z- m9 Z
- h F; l& X+ d0 y8 {/ L3)负责管理申报资料。
0 U- \. N$ @2 m6 Y9 P9 [" X9 s" _
0 a9 v. }8 ?9 s2 r/ e第十二条 生物部职责8 A; j* s& N% G* [0 A0 Z; t/ _
2 W7 z- Y$ P: W! R$ F! P1)负责生物技术人员的引进和培养
& M( e4 m* [3 u$ D6 F
3 W$ |: D! }* t6 L2)负责对项目的适应症及靶点风险进行评估,按月给出风险评估报告;
4 }$ a+ U- W3 x, ?" w5 j( W 3 d. O+ j `# R2 F
3)负责生物评价的平台建设;( g, X/ V; b$ d+ Y; c2 t9 J
4 [) a; n( H& Z0 t* ]4)对每个阶段进行有效性、安全性等生物评价,及时判定是否符合各阶段的生物标准。
0 N; z3 m5 T: @' o% x $ D- Y' C( L1 C6 x. e' G
第十三条 财务部职责7 \( N7 z5 t1 n$ S" t, G
1 O2 P% e! c- j: P5 `. w2 l2 a
主要负责审核项目的费用预算以及监督项目运行过程中费用的使用情况。
" O+ k+ s/ k) H6 P1 N: b$ U- M( ? 8 K; ~8 ? i8 C" I: R5 U0 C9 t
第十四条 项目经理职责
; m' G/ ?: a5 S
, y3 e; I5 M0 Y2 p) Z1)对项目使用的人、需要的财负有全部的选择和审批的权利
, Y1 P' i$ o4 R/ q2)对项目的计划、实施、监督与控制负有全权的责任;4 Z; ]' e. I* I
2)解决在项目过程中项目的内部矛盾,使项目顺利进行;9 A$ |: B4 [9 q
3)与企业的各个职能部门进行充分的沟通、协调,确保项目能顺利的进行;
5 L' x' n% h( y0 G4)协调企业内、外部的资源,并合理的分配和使用资源;5 C+ n2 K: \9 {8 ^' ^
5)形成良好的项目团队的合作模式;% G: {7 M _- \& v, u$ r0 j$ r) S
6)项目经理有责任和义务每月汇报项目的进展及风险情况。& }% S2 q% L1 Q& W0 X* Y
第四章 组织与实施* S1 P+ V( @/ s4 E+ v
* f# q" @! o5 ]' n) q第十五条 研发中心的同一个项目可以多个项目组平行开展,形成竞争机制,根据进度情况由项目评审委员会决定是否合并。. ?" c& ?% t+ I) ?
4 ~' s& k# Z- y0 q
第十六条 项目实施实行项目经理全面负责制。每个项目或/及每阶段必须明确一个项目经理,且在每个阶段开始时同时确定下一阶段的项目经理,最晚于项目本节点完成的3个月前确定下一阶段的项目经理。项目经理是项目的直接管理者,也是项目的直接执行者,归口于研发中心负责人。5 m" g0 F4 t4 E2 B( ~. g1 e! X
, F( W, Y- F% f! t第十七条 项目一经公司批准立项,一个月内公开竞聘项目经理。项目经理一经聘用,享受预发放项目奖为4000,6000,8000元/月/项目(依据国家项目分类而定)。项目结束后,项目经理任职自动结束。若项目在实施过程中,出现重大问题时,经过项目评审委员会讨论和判定,有权解除该项目经理,进行重新竞聘。
+ z: S2 X/ `8 p! l- v / F3 Q- t8 v! x- c8 T! ]# i( V
一个人承担多个项目,预发奖可累计发放。
2 O7 D" K% \( {- X1 _; Q7 q " `$ K# D# I! c2 n
第十八条 项目经理任职条件& m+ f; U7 ~0 A& F1 ]+ g
' F7 p: y) ]) Y, v* `" k 项目经理须本科毕业5年,研究生毕业3年以上,有较强的组织能力,具有本领域技术能力强者优先。
8 t& d/ B4 [) k3 n/ R, s) C/ r- M第十九条 项目经理一经聘用,享有充分的人事权和财权,首先负责组建团队,填写详细的《项目计划书》,确定项目的详细研究内容、进度计划及考核节点、人员使用及费用预算,《项目计划书》报项目评审委员会审批,审批通过后与研发负责人签订项目考核目标责任书,确定考核指标,其绩效按项目节点考核。项目目标考核责任书一式五份,公司战略规划部、人力资源部、财务部、项目管理部、项目组各执一份并上墙公布。项目进度节点时间非项目评审委员会同意不得任意更改。& w# H$ P, A: {0 Q7 C ~
, D% G1 g4 X; v/ V8 T& h8 ]
第二十条 项目管理部依据项目计划书,对该项目的过程和进度进行监督管理。9 E n, d9 C7 L" b
8 `# X8 p( O e3 g8 h8 T% N% X第二十一条 项目管理部负责帮助项目经理组织由项目经理主持的项目技术会议,并做好会议记录。技术会议每周组织一次,每两周进行一次由项目相关的学科领军人、首席研究员以上人员及外部专家参加的技术讨论会。
& V2 m5 y+ V8 q6 T2 A$ U w
! s( g! \% r# J: }' u! _) P第二十二条 项目管理部负责组织项目进度评审会议,项目进度评审会议每月一次,主要评审项目的先进性及竞争对手分析等议题。# U- S6 h' A$ y1 d
! S) r* E0 V+ f4 a( [第二十三条 项目管理部负责收集在研项目的月度、季度、各节点的进展报告,风险评估报告,根据报告,建议项目进度是否调整。. V' K6 h7 ?* D0 M% y9 U
9 o, Y: `: E: O7 \4 m( q; r9 A
第二十四条 项目有充分依据发生变更(目标、各节点、人员及预算等),项目经理可填写《项目变更(终止)申请》,并重新制定项目考核责任书,报研发中心负责人审批,经研发中心科研项目评审委员会审核批准执行,交由项目管理部备案。
. d* o' @+ ^7 m% A: I: T5 q( t5 j 8 O/ ]( s, J8 |( |9 B; C8 @
第二十五条 任何员工通过任何渠道了解到在研项目可能存在较大风险时,必须及时通知项目经理和项目管理部,项目经理必须立即向研发中心负责人汇报,同时报项目管理部备案,项目管理部负责上报科研项目评审委员会进行决策;2 T: f5 f/ w( E: _/ `7 R# Q$ g7 p
( C8 g) ]) G9 [6 x第二十六条 项目节点完成或终止后,项目经理填写《项目变更(终止)申请》报项目管理部,项目管理部依照《项目计划书》审核出具结论,并报研发中心负责人批准,两周内撰写项目结题报告,最终报科研项目评审委员会评审,确定项目是否推进与终止,最终结果报项目管理部归档。
9 q/ D% f0 I- c+ f3 L7 J
' c5 b# I; c: t5 _0 L" ~第五章 项目进度参考标准及考核目标
" M, s, V. s" T2 c- Y
3 H( x7 u( P0 z x3 I 研发中心所开展的项目包括:创新药项目、微创新项目、仿制药项目以及其他项目。创新药项目包括1类化学药、有专利权的独家生物药、微创新项目,仿制药项目包括化学药3类和6类,其他项目包括临床研究项目、合作引进、技术攻关、工艺改进等其他与药品相关的项目。
% [4 O- o" R# |0 N8 K / ?/ D; L+ R& ?* t4 N4 @# F) U
第二十七条 创新药各阶段项目节点的进度参考标准及考核目标参见下表。
( r: S( o& e$ U W \
+ F+ w' m; f( k" k% h* ]# `" Z9 g2 A
序 |
* E. u( A: U3 j4 C% }! j阶段 |
, _7 [1 f0 [+ v' p5 _6 ~! C8 P研发进度 |
) C+ ]$ F# S/ S4 @4 y* R进度要求 | ; j$ T' a: R; m. p. x
考核目标 |
( j' H7 W% a! C9 k3 {1 | & _$ X: ^$ v5 n7 F
研究阶段 |
5 P- C+ X# i- b- ~ I% C. Z) n概念验证 | 1 f: B2 I2 w+ j9 Z
≤0.5年 |
1 }( @/ L+ \3 V) U生物活性达到的标准/初步结论 |
8 w+ f8 U2 I1 f8 O0 v5 B& C2 |
0 w8 w5 }8 B8 J; R获得候选化合物 | ) \/ }1 l. r5 T R- V( z+ Y( l
≤1年 | . q9 {1 x4 c9 t: O& ~ {/ I
获得候选化合物 | $ ~; K5 E9 d( c4 a9 t" @
3 |
: F, i% m) X4 N6 l9 r, z开发阶段 | ; _6 p+ ]$ C. O
药学研究 |
+ K5 g% x5 }! e' n≤1年 |
2 M4 [( L! F+ J! M7 S完成药学申报材料(不含稳定性) |
! \# q y, T8 m1 z4 | : F8 Z* o. q( U Y9 @+ Z- g" A+ r
生物评价 |
8 U0 N6 }3 D& S$ a0 y* g≤10个月 | 5 T& D5 V9 y" _* ^3 @' A( d
完成生物评价申报材料 |
+ Y3 Q: g6 o3 Z |( G5 | r7 B, X/ w* I2 E; E5 Q8 K3 I8 a
注册阶段 | & S' ~6 R: Y4 Y" f( U @8 C2 s+ v
≤2个月 | 2 x j$ V! [. F
CFDA申请号 | . A) ]7 E& o5 }- \/ m. \
6 | ! ^" G) I4 l" D7 b; S3 S& ~
临床批件 |
) _$ J5 m$ o, E0 \≤1年 |
( i( y9 @$ s. y临床批件 |
8 H9 v5 g9 P/ H/ I* T9 \8 @" d: r/ N7 | 2 [! T4 p" O( K4 j8 h3 b7 m% T- |
| % T1 ]: _. Y+ c2 h% k
I期临床试验 | 2 v1 _: f( c) ^" I" X
≤1年 |
2 {; z/ U6 K" s2 m6 ACFDA补充申请号 | 6 g- |1 o7 ]2 `2 ~9 }
8 | - X- n: K% M( k- F+ Q8 F, u* B
|
& R2 I9 Y* G( b* `, tII期临床试验 | ! O2 C: S. G" G* w, k6 _! e: x
≤2年 |
) {1 H" [$ X- w# gCFDA补充申请号 | ! V' h* C1 v, s0 r9 B; N
9 |
8 \7 K1 O: J- C0 Q$ l, R |
& H6 a# t8 C* j( BIII期临床试验(申报生产) |
; y6 }6 @; \6 _/ _≤2.5年 |
6 \/ J! X, p4 W9 `申报生产受理通知书 | 2 |2 s# W! B5 p' T& r
10 |
9 a& ]3 W4 Q" e6 Y | ; o X: Z! ^& I1 E
取得生产批件/新药证书 | ( w/ `5 m1 L. \, l9 P7 {7 r9 J7 b6 p
≤1年 | / E, H8 S& o! ^, I! f7 f* T
生产批件/新药证书 |
5 ^ j) k" E& K# R合计 |
: c5 v: n8 X6 X; [8 J: y, E) G: j) B |
$ w, o6 b" e* g+ I/ Z |
- g+ ?/ s5 c' x0 {≤11年 | ; B7 z# w2 W) ?& V5 L% Y, `
|
( a( x# R+ U' a- q+ s) D! }1.药学研究阶段合成工艺研究进度参考标准
$ n# K0 ?2 }3 x8 E
, K' i/ |( J' u) J0 }8 a- C4 ?节点 | ! Y& l; L3 ~" c0 x* {1 l. l0 f
阶段 | 8 W- ^4 }+ ?$ t
研发进度 |
5 Z( y2 ]) q' T! ~! g2 K% i进度要求 |
# | r0 p, o% {/ E: T, v, j考核目标 |
, J7 X% x( l/ o0 n1 |
. k* O' ]# r; | q1 \工艺优化阶段 | ( ]# e1 N, I, l- g* t* z7 [
工艺路线确定、工艺优化、晶型研究和小试样品制备。 |
) E5 F- _3 n$ g8 p* u≤9个月 | 5 I; P, h, _6 E
完成2批百克级样品的制备,初步检验合格。 | ( j. L, c# U9 A/ s
2 | % t* k2 \& w, I* @3 O6 i2 W
中试样品积累阶段 |
" T& Y; ~* `" K% `5 ]! b工艺优化和中试样品制备。 |
) H( b" I( D9 @2 y4 O≤3个月 |
2 `9 \5 ?, N) V4 @完成申报所需量2批公斤级以上样品的制备,检验符合质量标准。 |
; @5 e8 [+ @/ R6 X& ?合计 | " Y5 t* W" i( j7 e# L' L! w; r
|
/ X0 t' Z! a8 F |
- {. M+ x9 \, h5 J1 m≤12个月 | . Y D. O+ k! d
|
4 V# v1 \( n# @3 L. r2. 药学研究阶段制剂工艺研究进度参考标准
+ I' m q# c6 [4 B9 o! ?
6 m8 m7 a+ A l+ K# Y) x6 s节点 |
\# k, g( |3 I) N) k; ?1 t J阶段 |
' r1 x# B% @$ ]7 o, r, Z研发进度 |
) K* Z# `6 t5 A" \% _进度要求 |
( F, U$ i3 J1 Z& O' T考核目标 |
3 T7 J1 r- T6 b: q: M1 t& h1 |
8 f, P6 G8 c% e! z. m3 E) G+ \) m. U处方工艺研究 | & D, M- R' g$ |' s$ r
确定处方工艺,小试样品制备及初步稳定性研究, | 5 N+ ]! _8 K& J+ {8 n. D B
≤5个月 | 2 A! w5 K+ B, A# c( n
完成小试样品制备及初步稳定性研究,原辅料相容性与处方工艺筛选。 |
8 l3 G" U3 @: _" `9 R) Z- N0 w5 W2 | % K$ F' s. \7 q; g0 w1 m# s
制剂工艺优化 |
$ S6 C- T/ r; ^, D, Q# |2 |工艺优化及中试样品制备 | 4 e8 a0 K# p% K. J# x; f7 ^
≤2个月 |
7 a& w# [' R1 R" n完成合格的中试样品 |
1 }% k7 C! x, x% l& c8 T; A合计 | ! _3 Z$ |: Z) d0 c8 c
| + P2 c& y0 M) w$ x+ Q: [# L; v$ ^2 \
| # c3 \7 w# k$ @/ p) ^0 h
≤7个月 |
& d7 D& W: ]! a$ y4 z6 D* ?* ]; l3 c3 J |
' v4 G: `* T' I, N. N第二十八条 仿制药项目进度参考标准及绩效考核目标" F7 A0 [0 e- ]
仿制药项目从立项到取得生产批件,整个研发周期:3类要求在6年之内完成,6类要求在5年之内完成。每个节点进度标准及绩效考核目标:8 T2 _" i- q6 ?4 N# c2 R6 G) b0 g
0 g0 n+ m0 |! j& E' h- {) D% v- D. }, m
仿制药3类 |
( V# K- r% h. K2 Q序 |
9 L: Z# N1 @+ C* ]; N3 U研发进度 | : }* a2 z* N3 m: V5 ?
进度要求 | # _+ w$ R0 Y3 R& E
考核目标 | R2 M3 {# F" ?/ e# `
1 | 2 l/ f# L7 \ ]0 r; Q4 i2 k& s) u
申报临床 |
/ b% _: D" |/ Y( W≤1.5年 | 3 k" p3 Z/ j* B i1 d; v7 I5 e
CFDA受理号 | 5 q5 L) r4 c. `" Y1 m2 _4 I
2 |
2 p& L8 r0 u H% C# l+ |1 F临床批件 |
7 E3 ~! o2 Y* b% }# E≤1年 |
; P# m; ?, W9 Q5 {2 m+ h$ o! F临床批件 |
7 P/ N4 U1 J$ H9 W( A6 H3 | ; s0 x7 p6 F f7 F8 N
临床研究 | % L5 R7 l5 U9 }7 M$ w& f/ g8 l
≤1.5年 | 7 m2 s+ I/ |5 w! f
|
+ t# Z- }; X; U# Z# D4 |
% T- N9 r, g0 q7 v2 v" K% f申报生产 |
3 E `$ ^. h/ a/ U1 X# F≤1年 |
) @# A" ~, c" z' W6 wCFDA受理号 | # Y, B. P2 Y5 F5 D, n
5 | $ f9 g0 D8 l# X1 s
新药证书 | / q3 Y" k) s1 D$ o: L& U
≤1.5年 | 5 h. n. J' e; U: u/ P
新药证书/药品注册批件 |
, l3 S5 F& c& C6 C合计 |
# P8 D& R4 _. d8 R7 e4 V' H | " R1 u% m7 b# y3 i/ n0 Y5 e# h
6.5年 | 6 Z) L2 z) X/ r4 s* P
| : g. i0 j: g/ I! [( { H
仿制药6类 | ! V$ h9 ^% f# r' s- S: ?8 f
1 |
3 [* s8 `) ^/ n+ U取得申报生产受理通知书 |
2 k6 `" {6 R* Q1 w+ D≤1.5年 | - s! F$ Z$ S+ a1 {( F0 o
CFDA受理号 |
- J `. G7 a, u; j3 d2 | 1 S$ B* p0 w% ^" u
取得生物等效试验批件 | 3 u2 e6 e: J1 I: a; }+ c3 s
≤1年 | 0 s! F0 u9 Z( E5 I
CFDA补充申请号 |
5 _/ b+ X. V1 |% Y( t$ B: x3 |
, k+ r' P6 [$ c% @( b8 `" E取得申报生产受理通知书 | & z% ?+ ] b8 p l0 A& O2 C
≤1年 | ) Y0 o6 C7 \, W- Y+ J9 p8 j3 c
CFDA受理号 |
3 r3 q3 t3 b- F7 x7 }4 |
+ v' K8 u _& e9 N$ _: A取得生产批件/新药证书 |
& k& ~% ^# R3 I8 z7 E/ w≤1.5年 | + h( X E1 n" M5 I. C) Z
药品注册批件 | 3 M5 s8 ~; H+ {& L! l
合计 | 1 y) ?$ O0 B* v: l' A
| ; r5 m( j; Z# g/ E+ s" v! ^
≤5年 |
) L! O8 b( p# y+ q0 Z |
/ U" `; _9 o- r6 S4 L# X1 z
第二十九条 其他项目进度标准及绩效考核目标
* ~' {7 N; X5 u8 j
* M. g7 N5 C4 I+ u 参照相应的进度标准
7 w7 i$ G, U# [ 备注1、临床试验,按当年的目标执行。8 p6 G5 {& n7 F
2、获得CFDA批件,由于药品审评进度受国家政策影响较大,获得批件的具体时间以项目执行期间国家实际审批时限而定。( }; @' d$ Z; J1 `8 {
第六章 风险管理- k% X7 K8 A- ]: h8 B( {
第三十条 专利人员对拟立项的项目给出是否立项的建议,以及专利风险利弊分析,制定专利战略及实施建议。专利人员对已立项项目及时掌控项目的知识产权风险,每个月及项目到达节点给出知识产权风险评估报告。/ C" \/ D9 r4 a5 ~; D! Y
第三十一条 市场部对申请立项项目进行市场预期预测,给出是否立项的建议。对已立项的项目及时预测判断项目的即时市场风险,并按时间节点给出市场即时风险评估报告。
* A% a9 \4 g" P第三十二条 商务部负责预测项目上市时产品的预期价格,以及产品上市后,由于市场份额竞争可能带来的价格预期。
6 }4 t5 M( O0 Q- M6 s& ~" F F第三十三条 生物部负责对项目的适应症及靶点风险进行评估,按月给出风险评估报告。
6 \% s# U; m( J4 Q第七章 人员管理) t( R% ~5 a( d6 P
第三十四条项目经理由公司任命,项目经理负责组建并管理高效的团队,项目经理和项目组成员一般都通过竞聘方式产生项目组长和组员,项目组可下设项目小组长。小组长不能明确3个月为单位考核周期的具体考核指标的享受预发放项目奖为1000-3000元/月/项目,有项目组经理提出建议报上级批准。组长和组员的任职期限、职责及考核由项目经理通过责任书予以约定。
6 L7 x" Z5 m7 W: V) r: a8 O& D每一项目组完成他的节点后,原项目组成员依据下一阶段项目的需求,由下一阶段项目经理决定部分或全部自动滚动进入下一阶段的项目组。2 a; z, `% B0 j' v# L7 g5 W6 k; ]
第三十五条 员工绩效合同的目标和考核标准由其上级会同他的直接客户制订,并得到直接客户(被服务对象)的认可,报其间接上级审批。项目经理根据项目的差异,制订直接下属组长或组员详细的考核指标及考核周期,考核周期可按月/季度及年度为单位。项目经理按项目节点完成的周期考核周期,给出组长或组员的考核绩效,报研发中心负责人批准执行。项目组下属人员的考核办法由项目负责人主导制定,项目组经理下属的考核的每个周期一般以1个月为一个考核单元,甚至可以再短,考核单位周期一般不可以超过3个月,每级人员的每个单元的考核表都上墙公布。9 m0 G( k: _9 ]6 a! r
第三十六条 对连续2个以上考核单元考核不合格的项目组成员,项目经理可退回原部门。退回员工技术职称降一级,由各科室主任负责进行专业培训;三个月内仍进不了项目组,则再次降级,6个月内进不了项目组则给予辞退处理。" G7 T; E/ M& P: E
项目经理可根据项目需要提出技术人员的引进计划,技术人员的引进和专业培训由各科室主任负责,提出申请后的6个月内各科室需满足项目组的需求。
5 n, a# e! ]( B: ]. S, b第三十七条 项目管理部负责项目组组长及成员的公示与变更管理。1 G& j$ Z, G7 n7 s- P
第三十八条 项目经理和科室主任对项目组成员的任职资格评审、职位升职、聘任等个人发展具有建议权,最终依据360度考评和绩效分决定是否晋升。
# p( N2 Q g# p9 \9 N) h- R第八章 经费管理9 H5 F, P, B5 F& D7 R
第三十九条 在项目计划书核准的范围内,项目经理享有本项目的费用分配和使用权;费用的使用遵循公司的费用审批流程,预算内的费用单笔2万元以内的实验费用由项目组组长批准即可请财务按财务规定支付。 第四十条 项目经费的使用必须严格执行公司的财务制度。项目经费主要用于项目实施过程中的人员费、设备费、材料费、图书资料费、试验费、燃油和动力费、会议费、差旅费、项目管理费及其它相关费用。项目经费的使用应做到合理安排,精打细算,专款专用。
4 w% Z/ V0 y1 o1 F6 A# Z. v& _' a1 {第四十一条 各类项目的费用目标 , s7 \) _8 F" E
项目经理根据所负责项目费用,详细分解包含人力成本和实验费用。各节点的费用暂定如下:
& c" _9 w# I' C$ c8 ^1) 1类创新药项目各节点总费用:
- y8 n0 L- K% d/ r, u7 `
# s4 m- u7 Y9 f: Y, X% b, A+ W4 }2 S; ?" |: i
2 o8 |8 o: M+ e% ^$ `0 P# |. w序 |
# ?, T; l0 l7 z7 }* P: }项目阶段性节点 | # t- I8 E4 u0 ^) a% N2 ?4 J
暂定项目节点总费(万元) | 2 A" a; L- I: t
1 |
; o- G: p& ~5 G6 V1 z; B0 u研究阶段 | , d; |. o. f& G+ S
≤300万;, a$ _! v# e% @/ k
试验约200-400万 | 4 V: y: t" O y
2 |
5 O8 e3 m' r" x9 p0 H: x临床前研究(申报临床) | ) I) h; y1 Y) |" w0 t) `% u5 s2 {
≤200万
6 K3 o2 g, B/ X+ f- [/ L试验费约600-1500万 | ( E) t7 F. ?! c1 n9 {7 F1 u2 G Y. c
3 | % q1 y8 N2 D5 i: T% O# K ^
I期临床试验 | . m+ N$ ]. x. r' @
经公司审核批准的预算费用(实验及人力资源费用分开预算) |
( j8 {4 ~0 I; C4 | + `5 x0 c& }' O+ d& e% D' r
II期临床试验 | . J2 M% A/ e: Z( {3 k2 |% I
经公司审核批准的预算费用 |
+ K9 p; I0 x& V- ]; Y3 s4 C& j) q5 | ; n) t5 P3 s8 m0 ?
III期临床试验(申报生产) | : p5 h5 }# X- C* v. `
经公司审核批准的预算费用 | : }1 }4 L! V. {& ~9 h7 N
6 |
7 U8 p0 j! Y4 D' t3 f6 ]取得生产批件/新药证书 |
+ P6 l" `6 z4 j! I' u经公司审核批准的预算费用 |
8 W( f3 M8 ^9 |/ b _8 ^2 ?
2) 3.1类化药项目总费用
( B; U# F1 p9 S8 Z: W6 _" j, X+ k
! w* M4 r" H& u/ J 项目取得申报临床受理通知书,人力≤150万,试验费100-300万,以项目经理竞聘上岗时批准的预算为准。
' ?5 y5 |2 P# ~9 A. ] ) _+ P7 X5 p s. C; h5 C. `$ U
3) 6类化药项目总费用8 S0 p; P0 y, ?" `* ^+ x
o3 j; O% w" P 项目取得申报生产受理通知书,人力≤150万,试验费200-300万,以项目经理竞聘上岗时批准的预算为准。
0 u! \' ]$ A- R; _# B1 F
& K/ s3 O8 u; R* u4) 其他项目的项目费用参照执行。" H2 I( N6 f j6 | r! ~6 T' s
; }0 W9 E7 D! c- z- j7 }- v" \
5) 人力资源费用完成节点结余部分全部用于项目组成员奖金
; E3 K$ f& [. |# V$ q8 \9 H * l$ e8 R- w- \: z
6) 实验费用超预算支出部分的使用需事先申请总经理批准后支付,预算结余部分全部归公司所有
8 e% g _0 e( H, J' t5 r 3 G# T! D5 C$ Z s3 [, l
7) 人力费用和实验费用对项目组来说仅指直接费用,不饱含固定资产折旧等。0 Z' i7 t1 u) S; T$ H0 t* V* W' C
# K- X5 Z5 O o- S8)人员培训及参加学术会议等调研费用计入人力资源费用
6 h; T4 ]# C9 S# ` C3 q2 }9 \+ Z& t9 A
第九章 资源管理 l2 W P' j* `$ D8 x
7 ?; q" q2 [: j1 _9 d+ Q# B3 ]第四十二条 项目经理根据项目列出所需平台及使用时间,由各分管部门负责人根据各项目进度,预先安排并做好按时使用的保障,平台的日常维护及构建由平台负责人负责。研发公共平台的建设由公司投入,独立核算,平台负责人参照外部模拟价格公布实验费用的统一价格,有项目组经理决定是否在公司内部平台实验,同价公司内部平台优先。; H' g+ u1 b. `0 H5 K; a9 o
) P5 a6 n! v( y第四十三条 仪器设备及平台出现交叉时,由各分管部门及平台负责人合理协调安排,出现争议时由研发中心负责人协调解决。
% U7 |# I8 K, Y4 V5 j z * k* ~0 E/ Q2 ^9 j9 I1 L
第十章 成果管理+ B. ?/ ]" x5 W7 R6 {
8 L1 E, s- ^; @; @5 p
第四十四条 研究成果为公司技术成果,归公司所有。任何人不得以个人名义向外涉密或转让。; s3 a& M( U* G: k/ H) F
0 w9 f( a$ r- W& f& M第四十五条 符合申请专利的均按照公司的专利申请制度执行;科技论文的发表按照公司及研发中心科技论文发表管理制度执行。6 g, ^/ Q: E; V- c) f
% D$ d2 a1 i: J
第四十六条 凡申报国家科技、省级、市级等科技奖项按公司科研项目申报管理办法执行。$ s5 j9 k; H# X6 d
( N: r% R+ M1 J% t# ^
第十一章 项目奖
# c# d4 w" C- X
( w* U" E* W! n# G" J第四十七条 项目奖金来源于项目已发直接人力费用的余额。项目经理的项目奖由他的直接上级出方案,报在上级批准,项目组成员的项目奖由其直接上级根据绩效确定出分配方案,并报其间接上级批准。
2 [8 e% u+ U [, ]; G* m5 p, X 3 f0 M: D, W+ N/ b' {& @2 v& \
第四十八条 在完成项目本节点任务时,发放项目奖总额的40%,其余60%至下一节点完成后发放。若下一节点不能通过,则不予发放。如果由于公司战略调整或外部环境(如阳性药临床失败导致原研公司终止)导致项目停止,则不影响该部分奖金的发放。
/ w0 e+ K$ U2 X2 j' G0 J- e# r* F
& D7 t; W# H3 E; s- ^( V" e3 i5 e第四十九条 项目奖发放额度,不因参与人员人数的该变而改变,参与人员越少,人均获得奖金额度就越大。3 y6 a G! A+ H2 }/ ~
9 H8 r/ q, _+ c% P4 F: t, ~
第五十条 员工如参与多个项目,则奖金可从多个项目中支出,加和发放,具体发放有个级人员的直接上级依据贡献拟定发放方案后报再上级批准即可。
- B' I; y: _' W5 g8 x
2 e) w* f+ x0 j5 R+ G0 m& W第十二章 项目效益奖励
9 s1 e# M* X/ U/ X0 g; D
4 {+ K- V2 `; A! R- S9 ]6 S1、创新项目,项目实现产业化后,在化合物(或用途专利)专利期内,每年该产品的销售额的2-5‰作为奖励,奖励项目组成员及项目的提出人员分享,发放方式同项目奖发放方式。3 G* g( q" P/ P8 i( i
* T& W v3 D6 V" O9 d" u! \) `2、仿制项目,上市后在药品的前三年,每年该产品的销售额的1‰作为奖励。* A8 }7 i' M4 w$ K' B7 k
9 x% \9 _+ v: }3、对于公司决定中止的项目奖励:若转让,则转让费除去本项目直接研究总费用后的1‰作为项目奖励。
- Z0 a* f* o& ~3 [! _2 v
; j* e; Y3 j1 C! j, c3 K4、创新项目取得阶段性成功后,如果转让,研发人员的奖励参照3执行。
1 U/ K) b" {- ~9 N4 Y
' W$ T5 G4 ]- M/ I+ l/ G6 x5、对于自身延期造成的项目中止,则不享受项目效益奖励。
% {8 s3 }* z8 Z1 ]' g$ B% f1 b; H! F9 E! f3 k: S. c# I
' M6 z. ^9 @8 L n8 T) {, Y% ?9 k: J% Q6 G* J, V
- b. r8 V6 G- d& H
0 c. U: T! f( f3 }7 q0 V/ B
附件一:圣和研发中心立项申请书5 d+ \9 w+ c$ l4 n* N" S7 j' L
& v" c% h }. k6 C" n+ S# c5 y附件二:圣和研发中心项目计划书
m6 _" h9 n! ^7 K6 s7 \3 o4 S; q( C* q! y% }6 ~
附件三:项目变更(终止)申请表; N! S9 ~) y" P# Z
3 Y2 B$ M- a' T3 \% ] $ V- |0 ~7 F/ G5 }- ^
9 F- i2 m9 x* J( t- K/ n
# `& F$ [/ U: m
$ |5 l' k+ v5 }$ |
; a5 h% \9 C* n4 o& i4 s2 j# b( f5 `9 s/ P* {$ H" O. @0 c$ x
: K4 v* H. G9 _5 z3 _
o3 Y) f9 ^& s6 E, _薪酬:% ]) B8 P) E! X& ~
; J. Q% z+ q+ q+ n$ DA:研发中心非技术人员的薪酬参照公司职能部门人员管理, y% p1 F3 J' _/ u/ |6 d
+ Z5 b3 a/ E! q, I . z, N2 m/ [( t. q3 D1 }
, Z0 I+ H" n8 g0 X* k) ?$ ?
B:研发中心技术人员薪酬:1 G: Q8 z7 ]) K
R' j# B8 \' r0 Q ]' t
研发中心技术人员薪酬包括基本工资和绩效奖金两部分组成。
: {5 h# ~: x& s; U$ I
. `$ o4 S, t' ]% F一:基本工资:
9 Z6 T2 B# m8 E& j7 J8 O! X, _6 m1 f: G( V7 Y- C {/ M3 O N
1:见习研究员:
# ]3 V, ]4 L4 x0 s1 \) K* A
' I" ` o% V/ m4 z应届本科毕业生一年内为见习研究员,一年内只要被项目组正式选用即转正为初级研究员;硕士、博士研究生半年内为见习研究员,半年内只要被项目组正式选用即转正为中级研究员,试用期内不合格或到期不能转正者则给予辞退。
/ G& G7 z5 h. Z0 x) F# `4 ?9 I) O5 h3 x1 o
(见习期的基本工资及各种福利不计入项目组人员费用,同时,见习研究员不参加考核,不发绩效奖)
) l# n6 n* O8 Z# a3 U. ^" L) t. i5 K- q
见习研究员基本工资:! h5 k* p( q: n& M8 b
5 ^0 q; U5 K% w" e本科生: 5000元
0 H9 b7 Y# G2 Q$ g
# s" C8 T! `% a' K硕士研究生:6000元
& h( @, T/ u0 `& ]4 C& T& Z$ ?0 O$ [/ I/ j
博士研究生:8000元
, x2 c0 {/ {! M5 T$ U# t6 P& k( _5 ~
" X# g) ^7 W; s) k/ x2:初级研究员:6000元
/ f* g8 W( C- y6 k0 ~0 K) B9 B
* x: P) T; O, O中级研究员:8000元+ F/ c! m) M7 D: f- _
7 M/ ~2 I4 T6 M9 d- N7 o7 Y
高级研究员:10000元(另每年有2万元的调研费用)
0 e$ T" _8 g, Q' p( K( V# l& f2 `- X" A9 L6 Q0 r6 |
资深研究员:15000元(另每年有3万元的调研费用)' M& Z6 j1 a% Q1 s9 s! `. |: O0 z
- q( i5 H' u! r2 e9 J3 j
专业首席科学家25000元(另每年有4万元的调研费用)8 r, t& g4 E' O% o8 C( [
( A9 D( U- F7 X K% b
* m1 ~- I& T& b! m" Q# s$ k8 s9 R& q' p
首席科学家40000元(另每年有6万元的调研费用)
, `5 E- I/ G/ b Z& V' @% X
0 ?+ ~4 l6 c) p调研费用)# c! x, |/ q9 v* B. J
& S) e* v" [" W' B; S
调研费用按实报销,项目人力资源直接费用有结余可增加此项费用
5 m8 t8 d: P0 T0 o1 n' }. d. v2 A- [" b8 U
6 T" I: F8 u( M7 {% b
+ N% G, r1 b# C, f/ o+ h$ b
特岗津贴另行制定办法
p, b% r" p8 L! \4 }0 @# j4 N, x4 O2 q5 |! p! g! n9 o
其他福利:
1 z3 ^4 m' m3 y: f, T% z- [7 t, a, k/ l4 D
1:公司对所有人员,每天提供免费的早、中、晚自助餐及21:00的宵夜
' g- t7 O& E3 N6 e# ~$ l9 G/ I7 e, M$ t3 O/ d, J' {
2:21:30后离开实验室可报销往返住地的打的费用,另外按公司的车改方案符合条件的可再次分享车改福利4 W& s2 V$ E3 M% E- [$ q/ t9 r! O
: f p2 A) A" K7 c2 ~: b! T6 y) T# a( c
3:家庭非工作所在地的员工按公司集体宿舍管理办法就近安排不同标准的集体宿舍
& Q: M+ ]5 R# T
8 a1 y9 D. P, h7 D, Z* D
7 u- W8 _" h% k& T3 Z, I n
0 F, W- y) F4 e- J2 j2 C$ a& G二:绩效奖金
7 b z7 {) [* q8 q) _* D2 z0 g6 ], M+ v& e) N; o7 F2 `
绩效奖金由项目组参照项目奖发放原则依据不同项目分别制定考核办法后发放。. e( v( ?0 a4 V. o$ J ]2 T: {& m
2 @5 v7 | Z# k! ?& f奖金发放原则:' z1 c; L2 o" o6 n* d
8 a3 A; ^( o' A
1: 考核指标:必须以量化的有效输出作为考核指标* t: ]4 X0 ?6 m" D
, e+ M1 S, f5 E' ]( l2:考核单位周期:
0 j$ C& h J4 s7 M
2 r! F, A. W% h1 j* E! ]! W2.1项目组组长:
# l/ `, E0 M. c9 i( ~6 `4 `; I; [% D Q4 R6 t
项目组长以他卸任组长为一个考核单位周期* n0 ~# {& s: s# P
% x; S9 a3 t4 a$ p; m
2.2项目组其他人员
6 f; q3 l* {" E# ]8 z8 T1 M' d/ S8 b& q* l0 A
初级研究员考核单位周期一般为一个月,不可超过3个月,可低于一个月4 k3 \. M, }4 n, N# ~! r' s# M
% T, J c; b; K! R1 X中级研究员考核单位周期不可超过3个月
% v& h3 ~& `8 [9 T8 J% q1 Z
& T7 h7 f" [, x& ^: M1 j* C' C高级、资深和专业首席研究员考核单位周期不可超过半年0 K1 W5 m, X* t/ L
3 T6 h! P8 U% e$ }6 B Z
考核单位周期结束即发全部或部分奖金,由项目经理依据不同项目不同考核内容而定
/ Q2 s& l# t% b2 k& O; i
# @' q: r( r, a比如:专门负责合成设计好的化合物的研究员,合成完成目标,项目经理就可选择给他全额发放。1 |0 B! k d5 f8 H# Q
3 H# D, X9 f7 b7 I3 }0 a& \
3:考核结果与奖金的关系; n2 T1 f+ h, g( i; Q3 |/ D
$ b0 u: G' ?; p0 r5 P
3.1:考核结果直接以得多少分计算,同时以1分对应100元; R& G6 [/ s% Z0 M. B
2 ]/ T7 A1 F/ \& }9 O; n, @比如:合成一个新化合物可发1000元即可对应合成一个化合物得10分6 y7 a( y( l x; _& }3 O. l
# @# e2 j2 Z* t每项工作的参考标准分值由项目管理部与各专业部门拟定一个范围公布,并供各项目组长制定下属人员的考核办法时参考用(另行制定), A1 F& `* c* G; V
6 F4 U$ e3 N0 C% N8 ^
3.2:每个不同级别的研究员每个考核周期必须有最低的绩效得分,低于最低分,得分归零,不再发放绩效奖
* f: f/ B4 g) H/ d# u9 T" v( P) T; W M" e! f# q" w$ e( K* Q1 p+ b
4:绩效考核合同签订后即上墙公布
( ~; U' v7 M3 K* L b8 F
0 y: V# w( o: N/ @ $ P+ d( V- A3 b; g: s; n0 p; K
8 c+ ?0 n9 o% f) a. p+ ~" w
p" G" J2 x: c( n# V+ p4 K# n* u! V5 x9 W; n8 r
晋升和降级; g+ @& O# T x3 u7 K% [) t) E
" w% K0 o: N0 a一:晋升
g( |7 i l% O/ ~. k9 x+ w
% a( E5 F2 H$ h. A( p" C0 t9 l价值观与公司一致且有绩效者的即可以晋升$ \! [, f, w: k9 E$ g6 Y1 O
8 b, f( ~) Y0 \: e. _- x: v价值观的一致性由360度评议而得
) U' Y6 P4 z0 V* `9 t. O. P, a* t# V# i
在价值观一致的前提下:) n$ t( v8 G0 j5 S( A& P
/ U0 a4 h( ]$ u" f
初级研究员绩效得分累计达 960分即可晋升中级研究员
# Z$ d7 {9 n- ^, Y& }' _
z: k* _8 z8 z1 I# _) n6 m中级研究员绩效得分累计达1200分即可晋升高级研究员1 d0 N" r0 G/ c) k) ~
, i2 o6 w# f( I8 Y
高级研究员绩效得分累计达1800分即可晋升资深研究员
; G+ \$ }, s9 b7 T. u( h/ A9 B: i- L* S7 O- U
资深研究员绩效得分累计达3000分即可晋升专业首席科学家
8 ]+ x* e/ t2 W5 I& r: |& z/ M+ M
专业首席科学家绩效得分累计达4800分即可晋升公司级首席科学家- g. m( C. D6 S$ n3 t" N6 d
$ ]0 S/ ~ }3 `' W2 a5 @* P5 N m" d二:降级! Z; i0 T/ V* I1 r/ P( l) b. r
" N. Y: ~" i6 B* H0 m1 }* b- q
各级人员既不能被聘任项目组组长,又不被项目组选用,前三个月内降级参加室主任组织的学习培训,3个月后仍未被选用,再次降级并继续参加室主任组织的学习培训,到6个月时仍然未能被选用者则给予辞退
5 L, Y* v' s7 ?, E7 S! ]- b
! n+ o5 E w2 g I7 ^各级研究员第一个考核周期考核分归零者由上级研究员及上级管理者给予指导,第二次出现考核周期内绩效归零者即给予降级,同时项目组有权要求其退出项目组" R- A4 v# {' w* f4 s% G9 v$ A
* `0 M4 q" A" `& X: |
高级研究员以上的研究员完成绩效分的同时需要完成项目选题的工作,如每个年度内未能完成年度目标,下一年度给予降级。自己立的项目在竞聘项目经理时,在评委打分的基础上可加5分参加竞争项目经理。) c3 q& `6 Q7 H+ t3 ?
. b! R' }- U* \1 `% t1 ]注:
. \2 u0 G0 C: ?& R$ ]" C; K1 {. C; L& Q7 G0 y- O( o
各专业科室主要是起到负责引进专业人才、组织资源培养项目组需要的专业人才的作用
4 J) s( [, n/ k) q
7 L+ K" y& L2 G! P+ }: N专业科室室主任须确保各项目组需要的专业人才在6个月以内能保证供给- Q7 E7 L& R" U8 t" D
: a: g! b( N8 x7 E& y7 O& l% E
室主任的岗位津贴:3000到5000元每月
+ d+ |) {; ^. I7 j* t6 P' n" U
: e3 I% [* E4 W' W" J7 m" N鼓励一人多职,各种薪酬累计变为他的薪酬8 |' F$ V9 w7 R8 @. C; _. |1 s8 }" H
2 x/ }6 v2 f) ? o, W) ]. M比如:一个人既是高级研究员,又是3个项目组的经理,还是室主任,则他的月基本收入=高级研究员的基本工资+每个项目作为经理的预发奖+室主任津贴 |
|